Donanemab 显著减缓患者认知和功能的下降
近半数 (47%) 的donanemab受试者(安慰剂组为 29%)在用药1 年后没有出现临床进展(定义为 CDR-SB评分 没有下降)
3 期试验达到了主要终点和所有评估认知和功能下降的次要终点
对比安慰剂,donanemab 治疗后减缓了患者临床下降达 35%,同时日常生活能力下降的速度减缓了 40%
超过一半的donanemab组受试者在治疗 12 个月时完成了研究药物的给药
印第安纳波利斯2023年5月4日 /美通社/ -- 礼来制药(纽约证券交易所代码:LLY)在今天宣布名为TRAILBLAZER-ALZ 2的 3 期临床研究获得了阳性结果,结果显示donanemab显著减缓了早期阿尔茨海默病患者认知和功能的下降。Donanemab 达到了基于阿尔茨海默病综合评分量表(iADRS)评估的从基线到18个月的主要终点。 试验的主要终点指标iADRS是评估患者认知和日常生活能力,例如管理财务、驾驶、参与兴趣爱好活动和谈论时事。同时,研究也达到了评估认知和功能下降的所有次要终点,并显示出与主要终点结果程度相似的具有高度统计学显著性的临床获益。基于这些结果,礼来将尽快开展全球范围内的递交工作,并预计在本季度内向FDA递交上市申请。此外,礼来将与 FDA 以及全球其他监管机构合作,推动药物尽快获批。
声明:
1、 该适应症为研究中的药品用法,尚未在中国大陆地区获批
2、 礼来不推荐任何未获批的药品/适应症使用
TRAILBLAZER-ALZ 2 是一项随机、双盲、安慰剂对照研究,旨在评估 donanemab – 一种试验性的靶向淀粉样蛋白斑块的疗法的安全性和有效性。该研究招募了患有早期症状性阿尔茨海默病 (AD) 的患者,包括AD源性的轻度认知障碍 (MCI) 和轻度痴呆阶段,并存在确证的AD神经病理的患者,受试者一旦达到预设的脑淀粉样蛋白斑块清除状态后即可被认为完成了donanemab的给药。
TRAILBLAZER-ALZ 2 研究的受试者在试验中会通过脑tau蛋白沉积水平(tau蛋白是一种可预测阿尔茨海默病疾病进展的生物标志物)进行分层。该研究的主要分析人群 (n=1182) 是由存在中等tau蛋白水平和阿尔茨海默病临床症状的受试者所组成,并具有足够的把握度。在该人群中,主要终点指标(iADRS)显示donanemab延缓了认知功能下降达35% (p<0.0001),且另一个重要的关键次要终点指标(临床痴呆评分, CDR-SB)显示18个月后donanemab延缓下降36% (p <0.0001)。其他预设的次要分析结果显示:
"在过去的 20 年间,礼来的科学家通过阐明 AD 病理的基本机制并发现能够探踪到AD病理的成像和血液生物标志物工具,在抗击阿尔茨海默病方面开辟了新的道路",礼来制药首席科学家兼礼来研究实验室总裁Daniel Skovronsky博士表示:"我们非常欣喜地看到 donanemab 在本次试验中获得了阳性的临床结果,对于参与试验的阿尔茨海默病患者而言,这一结果是令人信服的且具有统计学显著性。这是首个针对阿尔茨海默病的研究药物的3期研究能达到如此令人瞩目的结果——可使临床和功能的衰退减缓 35%。"
该研究还招募了少部分基线 tau蛋白水平高的受试者 (n=552),代表着疾病进展至稍后阶段的AD患者。由于预计这些受试者病程会进展得更快并且对治疗的反应会弱一些,所以该研究的目标人群是tau蛋白中等水平的人群。试验入组的这些tau蛋白高水平的受试者会和tau蛋白中等水平的受试者整合到一起进行额外的主要分析 (n=1736)。在这一整合人群中,donanemab 依然在所有临床终点(p<0.001)中都显示出有意义的阳性结果,CDR-SB 和 iADRS 评分分别显示donanemab可减缓 29% 和 22% 的下降。
试验中淀粉样蛋白相关性影像异常( ARIA )的发生率与2期研究 TRAILBLAZER-ALZ 结果一致。 ARIA在这一类清除淀粉样蛋白斑块抗体药物中都有观察到,最常见的表现是大脑一个或多个区域出现暂时性的肿胀 (ARIA-E) 或微出血或表面铁沉积 (ARIA-H),这两种情况都可以通过核磁共振成像检测到。在整个 donanemab 治疗组中,24.0% 的受试者发生 ARIA-E,其中 6.1% 出现症状性 ARIA-E。 ARIA-H 发生率在donanemab治疗组为 31.4%,而安慰剂组则为 13.6%。大多数 ARIA 病例为轻度至中度,并可在适当的治疗监测下消退或者稳定。 ARIA 通常没有症状,但可能会发生严重和危及生命的事件。在这项研究中,严重 ARIA 的发生率为 1.6%,包括两名归因于ARIA 而死亡的受试者和另一名在出现严重 ARIA 事件后死亡的受试者。 8.7% 的受试者发生了输液相关反应,大多数病例的严重程度为轻度至中度。
"我们因 donanemab 可能提供的潜在临床获益而感到鼓舞,虽然正如很多治疗使人衰弱和致命疾病的有效疗法一样,该疗法也可能存在严重且危及生命的相关风险",礼来制药神经退行性疾病领域研发副总裁、Avid Radiopharmaceuticals总裁Mark Mintun 博士表示: "我们注意到研究结果显示处于疾病早期病理阶段的患者可能对靶向淀粉样蛋白的治疗最有效。在此,我们感谢所有参与临床试验的受试者和他们的家人,和我们一起不遗余力地寻找这种疾病的解决方案。 "
TRAILBLAZER-ALZ 2研究表明,通过淀粉样蛋白正电子发射断层显像(PET)进行脑部扫描可观察到,除了减缓认知和功能下降外,donanemab早在开始治疗后 6 个月就显著降低了受试者脑内的淀粉样蛋白斑块水平,而且许多患者达到淀粉样蛋白病理阴性[1]( 在tau 蛋白中等水平人群中 ,34% 的受试者在 治疗6 个月时实现了淀粉样蛋白清除,71%的 受试者在 12 个月时实现了淀粉样蛋白清除)。
"淀粉样蛋白斑块是一个定义阿尔茨海默病疾病的病理生理学特征",TRAILBLAZER-ALZ 2 试验的研究中心之一,Banner Research首席执行官 Eric Reiman 博士表示,"这项研究的关键数据为去除淀粉样蛋白斑块与患者临床获益之间的关联性提供了令人信服的证据支持。"
"这些 3 期数据证实了我们在 TRAILBLAZER-ALZ 研究中所观察到的获益。这也意味着如果donanemab获得批准,将是早期症状性阿尔茨海默病患者治疗方式的里程碑,并将帮助他们继续参与有意义的活动。"礼来公司执行副总裁兼礼来神经科学总裁Anne White表示。 "我们相信我们的研究数据符合医疗保险和医疗补助服务中心 (CMS) 所描述的‘高水平证据',这也是重新考量其国家医疗覆盖指标的触发因素。患有早期阿尔茨海默病的患者需要并且应该获得全面的保障和已获批的疗法。"
关键研究结果表明:
在tau 蛋白中等水平人群中,基线特征与其他同期开展的早期症状性 AD 研究相似(例如,MMSE 评分为 22.9)。安慰剂组疾病进展如预期所示(iADRS 和 CDR-SB 在 18 个月内分别下降了 9.3 和 1.9 点)。预设的分析使用的标准统计方法包括重复测量混合模型 (MMRM) 和自然三次样条 (NCS) 分析,两种分析方法的结果类似。以下疗效指标显示了对比donanemab与使用安慰剂治疗的受试者在 18 个月时的下降情况:
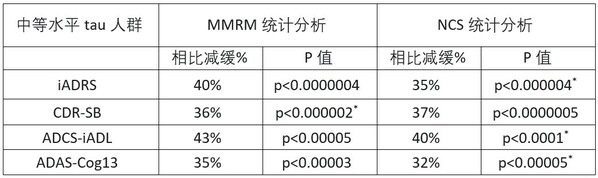
*表示alpha控制分析;iADRS= 阿尔茨海默病综合评分量表; CDR-SB= 临床认知症评分-总合;ADCS-iADL = 阿尔茨海默病合作研究 – 工具性日常生活能力量表(iADL); ADAS-Cog13 = 13项阿尔茨海默病指标-认知量表
在tau蛋白中等水平及高tau蛋白水平的整合人群中,基线 MMSE 评分为 22.3,安慰剂组与tau 蛋白中等水平人群相比表现出更大幅度的下降(在 18 个月内iADRS 和 CDR-SB分别恶化 13.1 和 2.4 分)。 18 个月时的研究结果显示:
TRAILBLAZER-ALZ 2 研究的完整结果将于 7 月在阿尔茨海默病协会国际会议上公布,并同期将于临床学术期刊上进行发表。
关于 TRAILBLAZER-ALZ 2和 TRAILBLAZER-ALZ 研究
TRAILBLAZER-ALZ 2(NCT04437511)是一项双盲、安慰剂对照的3期临床研究,旨在验证 donanemab 在患有早期症状性阿尔茨海默病(阿尔茨海默病源性MCI 或轻度痴呆)并存在AD神经病理证据的 60-85 岁受试者中的安全性和有效性。该试验招募了 1,736 名受试者,这些受试者基于认知评估结合淀粉样蛋白斑块和 tau 蛋白分期PET 成像进行筛选。
礼来在2021年披露并在新英格兰医学杂志(NEJM)上发表了donanemab2期试验TRAILBLAZER-ALZ研究的结果。此外,礼来还在 2022 年第 15 届阿尔茨海默病临床试验 (CTAD) 会议上披露了第一个针对早期症状性阿尔茨海默病的比较研究 TRAILBLAZER-ALZ 4 的研究数据。
礼来将继续在多项临床试验中研究donanemab,包括 TRAILBLAZER-ALZ 3——该试验的重点是预防临床前 AD 受试者发展成症状性阿尔茨海默病,TRAILBLAZER-ALZ 5——一项目前正在中国开展的针对早期症状性阿尔茨海默病的注册研究,和 TRAILBLAZER-ALZ 6——通过新的 MRI 序列、基于血液生物标志物和donanemab的不同给药方案来增强我们对 ARIA 的理解。
关于阿尔茨海默病
阿尔茨海默病是一种致命性的疾病,会导致记忆力和其他认知能力的进行性下降。阿尔茨海默病引起的痴呆是最常见的痴呆形式,占所有痴呆病例的 60% 至 80%[2]。目前,全世界有超过 5500 万痴呆症患者,预计到 2050 年,这一数字将增加到近 1.39 亿[3]。全世界每年新诊断出超过 1000 万例痴呆症病例,这意味着每 3.2 秒就有一例新病例,这极大地增加了社会和家庭的照顾负担。
关于礼来制药
礼来制药是一家从事药品研发、生产和销售的全球领先的医药公司,致力于通过创新改善人类健康水平。礼来制药诞生于一个多世纪之前,于1876年由礼来上校在美国印第安纳州创立,公司创始人致力于生产高质量的药品以满足切实的医疗需求。今天,我们仍然执着于这一使命,并基于此开展工作。在全球范围内,我们的员工始终努力研发能为人类生活带来改变的药物,并将其提供给那些切实所需的患者。不仅如此,我们还致力于改善公众对于疾病的理解、并更好地开展疾病管理,同时通过投身于慈善事业和志愿者活动回馈社会。礼来本着"植根中国,造福中国"的理念,着力拓展在华业务,在糖尿病、肿瘤、免疫、疼痛和神经退行性疾病等领域居领先地位。如果需要了解更多关于礼来制药的信息,请登录:www.lilly.com。
[1] 1. JAMA. 2011;305(3):275-283
[2] Alzheimer's Association. 2022 Alzheimer's Disease Facts and Figures. https://www.alz.org/media/Documents/alzheimers-facts-and-figures.pdf. Accessed May 12, 2022.
[3] Alzheimer's Disease International. Dementia Statistics. https://www.alzint.org/about/dementia-facts-figures/dementia-statistics/. Accessed May 12, 2022. https://www.alzint.org/about/dementia-facts-figures/dementia-statistics/. Accessed May 12, 2022.

